
过去几年里,免疫疗法的问世,极大改变了人类治疗癌症的格局:在免疫疗法的协助下,许多原本无药可治的晚期癌症也能得到长期控制,甚至是“功能性痊愈”。然而,肿瘤免疫疗法并非“万能药”,而是有其瓶颈。其中,最关键的一个瓶颈在于,只有20%-30%的患者对免疫疗法有反应。对于大部分癌症患者而言,免疫疗法并不起效。
令人奇怪的是,在患者的肿瘤周围,医生们依然能够发现许多免疫T细胞。但这些抗癌卫士却只是静悄悄地待在肿瘤旁,迟迟没有发动攻击,让人们百思不得其解。多年来,科学家们一直想要找到这一现象的背后原因。目前的主流观点认为,肿瘤微环境抑制了免疫T细胞的功能。

先前,癌症免疫专家Nicholas Restifo博士曾带领团队一探肿瘤微环境的奥秘。他们发现,死亡的癌细胞会释放高浓度的钾离子,而这些钾离子能让周围的T细胞丧失攻击癌细胞的能力。在今天的这篇论文里,研究人员们进一步拓展了他们的发现。而这一发现有望带来更好的免疫疗法。
首先,这支团队回答了钾离子为啥能够抑制T细胞的活性。他们发现,如果环境中的钾离子浓度过高,T细胞的代谢会受到严重影响,无法从周围环境里吸取营养,从而处于“营养不良”的状态。可以想象,连饭都吃不到的T细胞,自然无法有效抗击肿瘤。
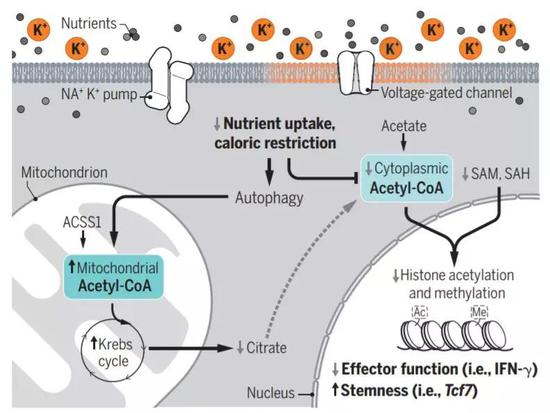
此外,研究人员们还发现了一个非常有趣的现象。在钾离子的影响下,T细胞的表观遗传学修饰会发生变化,影响T细胞的分化。于是,这些T细胞一直被束缚在“干细胞状态”之下,只会不断自我复制,却无法顺利分化成具有杀伤性的效应T细胞。这就能够解释,为啥聚集在肿瘤周围的大量T细胞会对病灶无动于衷。
理清生物学机理后,“干细胞状态”这五个字吸引了研究人员的注意。

原来,人们正在积极研发一种新型的免疫疗法——医生们期望从患者体内分离出肿瘤浸润的免疫T细胞,在体外不断扩增,并将T细胞大军输回患者体内,以求对肿瘤发起凶猛的攻击。这一疗法被称为“过继性T细胞疗法”,仅在少数患者中取得了成功。多项临床前和临床试验表明,T细胞的“干细胞状态”是这种疗法的成功关键。既然长期接触高浓度钾离子的T细胞还能保持“干细胞”的初心,它们能否带来更强力的过继性细胞疗法?
为了验证这一策略的可行性,研究人员们首先从多位癌症患者身上分离出了肿瘤浸润T细胞,并在富含钾离子的体外环境中进行扩增。研究证实了他们的猜测——尽管钾离子在肿瘤微环境中会抑制免疫T细胞的活性,但它给过继性细胞疗法带来的收益却更为明显:这些T细胞的一些关键生物标志物水平明显升高,预示它们可能具有更强的疗效。
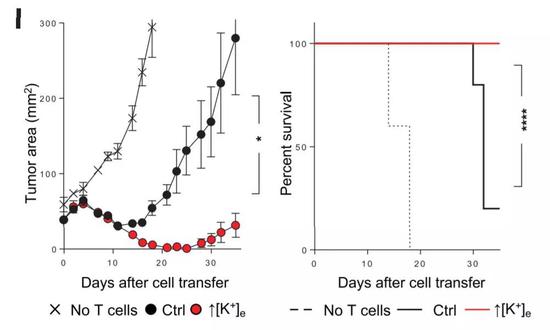
在小鼠体内,这些细胞的疗效也得到了证实。同样是经过钾离子的处理后,扩增的T细胞被输注回了黑色素瘤小鼠体内。研究发现,没有接受任何T细胞输注的小鼠,不到20天就全部死亡;接受普通T细胞输注的小鼠虽然活得更久,但在治疗的30多天后,死亡率就接近80%。相比之下,已经在体外历经过钾离子洗礼的T细胞,面对恶劣的肿瘤微环境,展现出了惊人的治疗效果。30多天后,小鼠的存活率高达100%,肿瘤面积也得到了很好的控制。
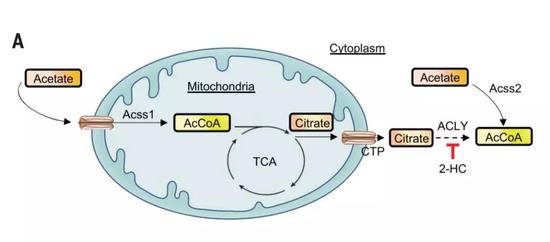
更令人欣喜的是,通过对背后生物学通路的理解,我们有望直接使用药物,达到同样的效果。研究人员们发现,通过直击这条通路里的关键酶,一种叫做2-HC的分子也可以提高T细胞的抗癌效果。
同样是在小鼠模型里,没有接受T细胞的小鼠在20天左右全部死亡,接受了普通T细胞输注的小鼠,在50天左右全部死亡。
而当T细胞接受了2-HC处理,并输注到小鼠体内的50天后,这些小鼠的存活率同样达到了100%!
“本研究帮助我们更好地理解了癌症免疫疗法的机制,也有望让免疫疗法变得更好,更为持久。” Restifo博士说道。《科学》杂志的专文评述也指出,该研究带来了增强免疫疗法的新策略。
未来,这群科学家期望启动临床试验,检验这一疗法在人类患者中的治疗潜力。我们期待早日听到好消息!